광동제약 "자진 회수 중"...지난달 17일 이후 출하 제품 안전
광동제약이 자사가 제조·판매한 혈관보강제에서 불순물이 검출돼 자진 회수에 나섰다.
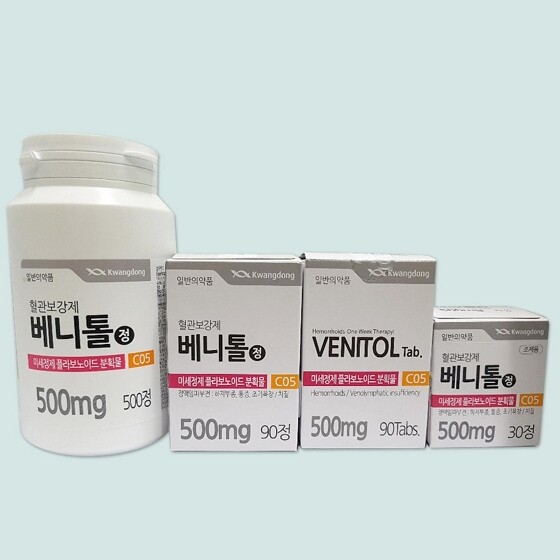 |
| ▲ 베니톨정 [광동제약 홈페이지] |
식품의약품안전처는 광동제약의 ‘베니톨정’에서 1일 섭취 허용 기준을 초과하는 양(127ng/일)의 니트로사민계 불순물(니트로소모르폴린· NMOR)이 검출됐다고 11일 밝혔다.
NMOR은 의약품 불순물 ‘니트로소아민류’ 중 하나로, 주원료에 사용되는 물질인 ‘모르폴린’과 부원료(부형제)에 잔류한 ‘아질산염’이 반응해 비의도적으로 발생하는 것으로 알려져 있다.
식약처에 따르면, 이번 안전성 조사는 유럽의약품청(EMA)에서 해당 성분이 함유된 의약품에 불순물 NMOR이 1일 섭취 허용량을 초과해 검출된다는 해외 안전성 정보에 따라 진행됐다.
조사 결과 해당 제품이 NMOR 1일 섭취 허용량을 초과한 것으로 밝혀졌고, 이를 제조·판매한 광동제약은 일부 제품에 대해 자발적으로 회수하고 있다.
식약처는 “지난 2월 17일부터는 NMOR이 1일 섭취 허용량 이하로 확인된 제품만 출하하고 있다”고 설명했다.
광동제약도 입장문을 내고 “2019, 2020년 제품은 예방적 차원으로, 2021년 제품은 일부 자진 회수로 진행된다”며 “이번 회수에 따라 현재 국내에 유통되는 베니톨정은 모두 안전성이 확보된 상태”라고 해명했다.
| ▲ 출처=식품의약품안전처 |
또 식약처는 “NMOR 1일 섭취 허용량을 결정하기 위해 중앙약사심의위원회 자문을 거쳤다”며 “의약품 분야 국제 가이드라인(ICH M7)을 적용해 127ng/일로 설정했다”고 밝혔다.
이어서 “현재 ICH M7에서는 발암성이 확인되지 않은 ‘변이원성 불순물’에 대해 평생(70년) 동안 매일 섭취했을 때 ‘무시가 가능한 수준(10만 명 중 1명 이하)’을 1일 섭취 허용량으로 정하고 있다”고 덧붙였다.
식약처가 NMOR 1일 섭취 허용량을 초과해 검출된 의약품을 복용한 환자의 건강상 영향을 평가한 결과, 전 생애 동안 추가로 암이 발생할 가능성은 10만 명 중 0.382명으로 나타났다.
이번 평가는 국제 기준인 ICH M7에 따라 이 제품의 허가일인 1994년 7월부터 올해 말까지 최대량을 복용한 것으로 가정해 수행했다.
식약처는 해당 제품의 처방받은 환자들이 복용을 임의로 중단하지 말고 의·약사와 계속 복용 또는 대체 의약품으로 전환 여부 등에 대해 상담할 것을 권고했다.
건강상 우려로 교환이 필요한 경우 남은 의약품을 가지고 조제 받은 약국에 방문하면 교환을 받을 수 있고, 다른 약국에서도 상담 후 교환할 수 있다.
[메가경제=이석호 기자]
[ⓒ 메가경제. 무단전재-재배포 금지]