백신 및 치료제 연구용 등 55개 기관에 변이주 536건 분양
델타 변이 속칭 인도발 코로나19 변이 바이러스 확산 공포가 전세계를 엄습하고 있는 가운데, 국립보건연구원은 델타형 변이바이러스에 대한 국산 항체치료제 효능 평가를 위한 동물실험을 진행 중이다.
국립보건연구원 권준욱 원장은 3일 코로나19 예방접종대응추진단 정례브리핑에서 “델타형 변이주에 감염된 동물모델(실험용 쥐)에 항체치료제를 투여하고, 이에 따른 치사율 및 바이러스 검출 양상 등을 분석하고 있으며, 결과가 나오는 대로 발표하겠다”고 밝혔다.
 |
| ▲ 코로나19 확진 해외 유입 사례가 증가함에 따라 델타형 변이 바이러스에 대한 우려가 커지는 가운데 2일 인천국제공항 제2터미널 코로나19 검사센터에서 의료진이 검체 채취를 하고 있다. [영종도=연합뉴스] |
권 원장은 또 “연구원은 민관협력을 통해 전 세계에서 발생하는 다양한 변이바이러스에 대해 광범위 효능을 갖는 치료제를 개발하고 있으며, 변이바이러스에 대한 효능 분석 및 국내.외 치료제 개발 동향 모니터링을 지속적으로 수행할 계획”이라고 덧붙였다.
권 원장은 이날 브리핑에서 1일 0시 기준으로 코로나19 치료제 투약현황도 설명했다.
먼저, 코로나19 치료제인 ‘베클루리주(렘데시비르)’는 현재까지 128개 병원 8621명의 환자에게, 또 코로나19 항체치료제인 ‘렉키로나주(레그단비맙)’는 현재까지 82개 병원 5529명의 환자에게 각각 투여됐다.
렘데시비르는 당초 미국 제약사 길리어드사이언스가 예볼라 치료제로 개발된 항바이러스제였으나 코로나19 발생 후 세계 최초 치료제로 인정받았다.
지난해 5월 1일 미국 식품의약국(FDA)이 코로나19 치료제로는 처음으로 긴급사용승인을 허가했고, 우리나라에서는 지난해 6월 3일 특례 수입을 결정했으며 같은 해 7월 25일부터는 품목허가했다.
렉키로나주는 셀트리온이 개발한 국내 최초 코로나19 치료제다. 식품의약품안전처는 올해 2월 5일 렉키로나주의 국내 조건부 허가를 결정했다.
또, 혈장치료제는 임상시험 목적 이외의 치료목적으로 47건이 식약처로부터 승인받아 사용 중이라고 권 원장은 설명했다.
‘임상시험 목적 이외의 치료목적’이란 다른 수단이 없거나 생명을 위협하는 중증 환자 등의 치료를 위해 허가되지 않은 임상시험용 의약품이라도 사용할 수 있도록 하는 제도다.
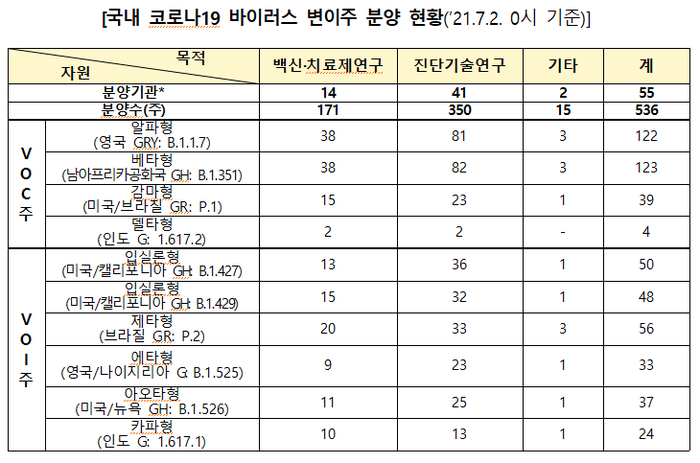 |
| ▲ 국내 코로나19 바이러스 변이주 분양 현황. [출처=질병관리청] |
권 원장은 이날 브리핑에서 국가병원체자원은행(NCCP)을 통해 분양된 코로나19 바이러스 변이주 분양 현황도 설명했다.
이날 0시 기준으로 변이주는 총 55개 기관에 536건이 분양됐다. 활용목적별로는 백신 및 치료제 연구용 171건, 진단기술 개발용 350건, 기타 융합연구 등으로 15건을 각각 나눠줬다.
536건 중 288건은 알파형(122), 베타형(123), 감마형(39), 델타형(4) 등 ‘주요 변이주(VOC)’이고, 248건은 입실론형(98), 제타형(56), 에타형(33), 아오타형(37), 카파형(24) 등 ‘관심 변이주(VOI)’이다.
권 원장은 “국가병원체자원은행은 신규 변이주를 신속하게 확보해 적극적으로 자원 정보를 제공하고, 분양을 더욱 활성화하여 보건의료 산업 발전에 기여하겠다”고 밝혔다.
[메가경제=류수근 기자]
[ⓒ 메가경제. 무단전재-재배포 금지]









